Personalização de imunoterapias baseadas em células T usando a nova tecnologia ‘SNAPtag’
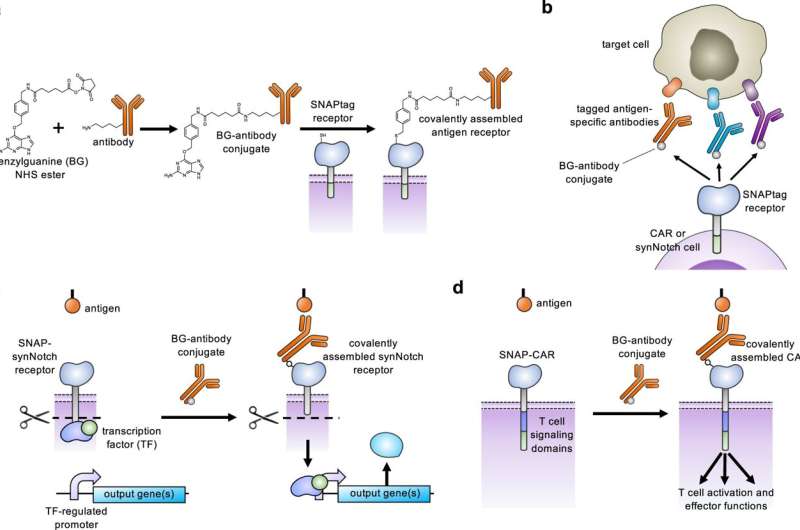
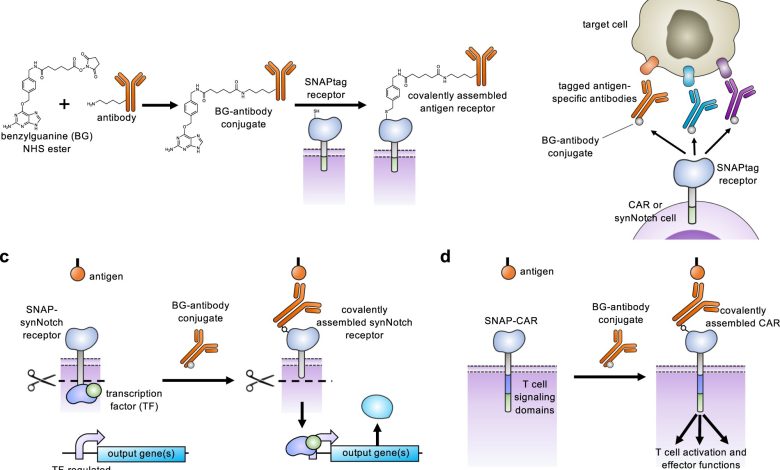
Adaptador universal SNAP-CAR e função de receptor SNAP-synNotch. a Um motivo de benzilguanina (BG) é conjugado quimicamente a um anticorpo usando um éster NHS de benzilguanina. O conjugado BG-anticorpo então se liga covalentemente à enzima SNAPtag extracelular por meio de uma reação de automarcação. b Os receptores SNAPtag permitem o direcionamento de vários antígenos diferentes usando o mesmo receptor, combinando células receptoras SNAP com diferentes anticorpos conjugados com BG. c O receptor SNAP-synNotch é direcionado por um anticorpo conjugado com BG e após o reconhecimento do antígeno leva à clivagem do receptor synNotch, liberando o fator de transcrição e a regulação transcricional de um gene ou genes alvo. d O SNAP-CAR é direcionado por um anticorpo conjugado com BG para ativar a sinalização de células T e as funções efetoras após o reconhecimento do antígeno. Crédito: Natureza Comunicações (2023). DOI: 10.1038/s41467-023-37863-5. https://www.nature.com/articles/s41467-023-37863-5
Pesquisadores da Universidade de Pittsburgh desenvolveram um sistema receptor universal que permite que as células T reconheçam qualquer alvo da superfície celular, permitindo células T CAR altamente personalizáveis e outras imunoterapias para o tratamento de câncer e outras doenças. A descoberta pode se estender a tumores sólidos e dar a mais pacientes acesso aos resultados revolucionários que a terapia com células CAR T produziu em certos tipos de câncer de sangue.
Descrito em um Natureza Comunicações estudo publicado hoje, 9 de maio, a nova abordagem envolve a engenharia de células T com receptores portadores de um “SNAPtag” universal que se funde com anticorpos direcionados a diferentes proteínas. Ao ajustar o tipo ou a dose desses anticorpos, os tratamentos podem ser adaptados para respostas imunológicas ideais.
Os pesquisadores mostraram que sua abordagem SNAP funciona em dois receptores importantes: os receptores CAR, um receptor sintético de células T que coordena um conjunto de respostas imunes, e o SynNotch, um receptor sintético que pode ser programado para ativar praticamente qualquer gene. Com a adição do SNAP, as possibilidades de terapias personalizadas tornam-se quase infinitas.
“Mostramos pela primeira vez que podemos fazer um receptor SynNotch universal. Este sistema SNAP-SynNotch é super programável porque você pode ter entrada de designer e saída de gene de designer”, disse o autor sênior Jason Lohmueller, Ph.D., professor assistente de cirurgia e imunologia na divisão de oncologia cirúrgica da Pitt School of Medicine e investigador no UPMC Hillman Cancer Center. “Nossa esperança é que possamos usar essa abordagem para fazer terapias celulares e fornecer genes para câncer, distúrbios autoimunes, tolerância a transplantes de órgãos e muito mais”.
A imunoterapia com células CAR T envolve a engenharia das próprias células do paciente para que o receptor de células T reconheça uma proteína específica nas células cancerígenas antes de infundi-las de volta no paciente.
“Um dos grandes problemas com a terapia CAR T é que você visa apenas uma proteína”, explicou Lohmueller. “Se o tumor evoluir para perder essa proteína ou diminuí-la, você precisa reprojetar as células T uma segunda vez, o que é um processo altamente complicado e caro”.
Para superar este problema, Lohmueller, primeiro autor Elisa Ruffo, Ph.D., associado de pós-doutorado em Pitt, Alexander Deiters, Ph.D., professor de química em Pitt e seus colegas desenvolveram células T SNAP-CAR universais adicionando uma enzima SNAPtag ao receptor CAR. Essas células são administradas junto com anticorpos direcionados ao câncer que são marcados com uma molécula chamada benzilguanina.
Por meio de uma química bioortogonal – um tipo de reação que ocorre em sistemas vivos sem interferir nos processos naturais – o SNAPtag reage com a benzilguanina, fundindo o anticorpo ao receptor. A adição de diferentes anticorpos, ao mesmo tempo ou um após o outro, permite que o receptor reconheça diferentes características do tumor.
“O que é único em nossa abordagem é como a célula T interage com o anticorpo. Não é apenas ligação, mas fusão via ligação covalente – a forma mais forte de ligação química”, explicou Lohmueller. “Este tipo de abordagem bio-ortogonal demonstrou funcionar em animais para fins de imagem, mas estamos entre os primeiros a usá-lo terapeuticamente, então estamos realmente ultrapassando os limites da tecnologia covalente”.
Uma vantagem dessa ligação forte significa que a ativação do receptor pode ser alcançada com doses mais baixas de anticorpo, disse Lohmueller. Usando modelagem matemática, o aluno de pós-graduação Adam Butchy e Natasa Miskov-Zivanov, Ph.D., professor assistente de engenharia elétrica e de computação na Pitt’s Swanson School of Engineering, mostraram que também pode ser possível obter atividade de interações mais fracas entre anticorpos e células tumoraisdando maior flexibilidade aos tipos de proteínas cancerígenas que podem ser direcionadas.
A ligação covalente também foi o ingrediente secreto para a criação de células SNAP-SynNotch. Quando um receptor SynNotch é ativado, forças de tração mecânica esticam o receptor para expor parte da proteína, que é então cortada para liberar um fator de transcrição que viaja até o núcleo da célula para ativar a expressão de um gene escolhido.
“Descobrimos que precisávamos da força de uma ligação covalente para tolerar essa força de atração”, explicou Lohmueller. “Se tivéssemos apenas ligação entre o receptor e o anticorpo, o receptor se separaria e não teríamos sinalização.”
Os pesquisadores mostraram que seus receptores universais SNAP-CAR e SNAP-SynNotch podem ser ativados em resposta a diferentes alvos, adicionando os anticorpos correspondentes. As células T SNAP-CAR também foram capazes de direcionar simultaneamente várias proteínas em diferentes tipos de células, sugerindo que elas poderiam ajudar a evitar a recidiva do câncer devido à variação nos alvos do tumor ou à perda desses alvos.
Em um modelo de câncer em camundongos, o tratamento com células T SNAP-CAR reduziu os tumores e prolongou muito a sobrevida, uma importante prova de conceito que prepara o terreno para testar essa abordagem em testes clínicos em parceria com a Coeptis Therapeutics, que licenciou a tecnologia SNAP-CAR da Pitt.
Mais Informações:
Elisa Ruffo et al, Montagem covalente pós-translacional de receptores CAR e synNotch para direcionamento de antígeno programável, Natureza Comunicações (2023). DOI: 10.1038/s41467-023-37863-5. www.nature.com/articles/s41467-023-37863-5
Fornecido por
Universidade de Pittsburgh
Citação: Personalizando imunoterapias baseadas em células T usando a nova tecnologia ‘SNAPtag’ (2023, 9 de maio) recuperada em 9 de maio de 2023 em https://medicalxpress.com/news/2023-05-customizing-cell-based-immunotherapies-snaptag-technology. html
Este documento está sujeito a direitos autorais. Além de qualquer negociação justa para fins de estudo ou pesquisa privada, nenhuma parte pode ser reproduzida sem a permissão por escrito. O conteúdo é fornecido apenas para fins informativos.
Segue as Notícias da Comunidade PortalEnf e fica atualizado.(clica aqui)