Nova abordagem previne danos hepáticos em modelos animais da síndrome de Alagille

Crédito: Unsplash/CC0 Public Domain
A síndrome de Alagille, uma doença genética que afeta 1 em cada 30.000 indivíduos, é causada por mutações no gene JAG1 na maioria dos casos. As mutações afetam vários órgãos, incluindo o fígado, onde muitas vezes resulta em colestase, uma condição na qual o fluxo de bile do fígado para ou diminui, levando ao acúmulo de bile que, com o tempo, causa danos ao fígado. Os tratamentos atuais concentram-se em retardar a progressão da doença; a única cura para a doença hepática na síndrome de Alagille é o transplante de fígado.
Pesquisadores do Baylor College of Medicine e instituições colaboradoras descobriram uma estratégia que evita danos ao fígado em modelos animais da síndrome de Alagille. Publicado na revista hepatologiaa abordagem abre a possibilidade de uma nova abordagem terapêutica para a doença hepática da síndrome de Alagille e potencialmente algumas outras condições associadas ao acúmulo de bile.
“Uma das principais funções do fígado é drenar a bile, que flui para o intestino para ajudar a absorver gorduras e eliminar toxinas”, disse o autor correspondente Dr. Hamed Jafar-Nejad, professor de estudos moleculares e genética humana em Baylor.
Um fígado saudável drena a bile através de uma rede de dutos chamada árvore biliar, mas certas condições como a síndrome de Alagille, infecções, toxinas ou lesões podem reduzir o número de dutos na árvore biliar, às vezes para menos da metade do que normalmente está presente no fígado. um fígado saudável. Menos dutos, clinicamente conhecidos como escassez de dutos biliares, significam menos drenos biliares do fígado, o que resulta em colestase que leva a doença hepática.
Os tratamentos atuais se concentram na correção de deficiências nutricionais, reduzindo o acúmulo de bile e aliviando a coceira intensa causada pela colestase para melhorar a qualidade de vida e retardar progressão da doença.
Para estabelecer uma nova abordagem para melhorar a colestase na síndrome de Alagille, a equipe trabalhou com três modelos animais da condição que haviam relatado anteriormente. O primeiro modelo foi geneticamente modificado para não ter uma das duas cópias normais do gene Jag1 (semelhante aos pacientes com síndrome de Alagille) e apresentava um defeito moderado no desenvolvimento das árvores biliares. Os outros modelos foram desenvolvidos pela manipulação de um segundo gene nos fígados do primeiro modelo, o que resultou em defeitos graves a muito graves no desenvolvimento da árvore biliar.
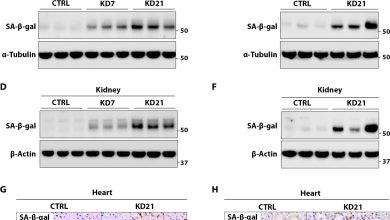
Curiosamente, o grupo Jafar-Nejad havia mostrado anteriormente que a remoção genética de uma cópia de outro gene chamado Poglut1 em seu primeiro modelo de camundongo com síndrome de Alagille melhorou significativamente a escassez do ducto biliar. No entanto, não se sabia se a redução da atividade do gene Poglut1 após a ocorrência de defeitos biliares ainda seria benéfica nesses modelos. Neste estudo, os pesquisadores investigaram se a redução do POGLUT1 nível de proteína após o nascimento usando uma abordagem diferente também melhoraria o desenvolvimento da árvore biliar.
A equipe trabalhou com a Ionis Pharmaceuticals, uma empresa pioneira no uso de oligonucleotídeo antisense (ASO) para tratar doenças humanas. A equipe Ionis projetou e gerou um ASO específico para o mouse Poglut1. ASOs são pequenos trechos de DNA modificado – às vezes contendo segmentos semelhantes a RNA – que são comumente usados para reduzir a quantidade de uma proteína específica no corpo (neste caso, POGLUT1) interferindo no processo que produz a proteína. ASOs já estão em uso clínico para tratar algumas doenças, mas, até onde os pesquisadores sabem, nenhum ASO foi aprovado pela Food and Drug Administration para tratar uma doença biliar.
“Nossos modelos de camundongos com anormalidades biliares moderadas a profundas receberam duas injeções pós-natais de ASO, que por sua vez reduziram a atividade do gene Poglut1 que produz a proteína no fígado”, disse Jafar-Nejad. “É importante ressaltar que o tratamento melhorou significativamente o desenvolvimento do ducto biliar e a formação da árvore biliar e preveniu a fibrose e a morte celular no fígado sem efeitos adversos”.
Ensaios de sinalização baseados em células indicaram que a redução do nível da proteína POGLUT1 promoveu um aumento na quantidade de proteína JAG1 e na sinalização mediada por JAG1, que provavelmente é o mecanismo pelo qual o ASO melhorou a árvore biliar mal desenvolvida em todos os três modelos animais.
“Estamos entusiasmados com essas descobertas, pois elas mostram que é possível promover a formação de uma árvore biliar quase normal em animais que já sofrem de escassez significativa de ductos biliares”, disse Jafar-Nejad.
“A síndrome de Alagille é uma das causas genéticas mais comuns de colestase em crianças. Embora muito mais trabalho precise ser feito para demonstrar a eficácia dessa abordagem para tratar a condição humana, nosso estudo oferece pela primeira vez uma potencial opção terapêutica para esses pacientes que dispensa a necessidade de transplante de fígado. O pensamento de que crianças que sofrem com essa condição podem encontrar alívio sem transplante nos mantém motivados a trabalhar no projeto”, disse o segundo autor Duncan Fox, aluno de pós-graduação do laboratório Jafar-Nejad.
“Nosso estudo pode ser útil não apenas para o tratamento da síndrome de Alagille, mas também pode beneficiar pacientes com outras condições envolvendo acúmulo de bile”, disse o primeiro autor, Dr. Nima Niknejad, um associado de pós-doutorado no laboratório Jafar-Nejad enquanto trabalhava no este projeto e atualmente é cientista sênior da Nitto BioPharma.
Mais Informações:
Nima Niknejad et al, Silenciamento de oligonucleotídeo antisense de uma glicosiltransferase, Poglut1, melhora os fenótipos do fígado em modelos de camundongos da síndrome de Alagille, hepatologia (2023). DOI: 10.1097/HEP.0000000000000380. pubmed.ncbi.nlm.nih.gov/37021797/
Fornecido por
Faculdade de Medicina de Baylor
Citação: Nova abordagem previne danos hepáticos em modelos animais da síndrome de Alagille (2023, 7 de abril) recuperado em 7 de abril de 2023 em https://medicalxpress.com/news/2023-04-approach-liver-animal-alagille-syndrome.html
Este documento está sujeito a direitos autorais. Além de qualquer negociação justa para fins de estudo ou pesquisa privada, nenhuma parte pode ser reproduzida sem a permissão por escrito. O conteúdo é fornecido apenas para fins informativos.
Segue as Notícias da Comunidade PortalEnf e fica atualizado.(clica aqui)